
Székely Zoltán
A HIV és gazdasejtjei kölcsönhatásának szerkezeti biokémiája. Kötõdést gátló molekulák modellezése, szintézise és biológiai vizsgálata
Szent-Györgyi Albert Orvostudományi Egyetem
Szeged, 1996
A disszertáció célja a HIV-1 külsõ glikoproteinje (gp120) és receptora (CD4) kölcsönhatásának tanulmányozása volt. A CD4-gp120 komplex képzõdés gátlásának mindkét lehetõségét vizsgáltuk:
(i) négy poliszulfonált azo-festék és a suramin CD4-hez történõ kötõdését, áramlási citometriával valamint szincicium gátlási tesztben vizsgátuk. A vegyületek inhibíciós sajátságait molekula modellezéssel értelmeztük.
(ii) pozitívan töltött aminosavakat tartalmazó ciklopeptideket szintetizáltunk a CD4 szerkezetének utánzására, a CD4-gp120 kölcsönhatás kompetitív gátlására.
Poliszulfonált festékek kötõdése a CD4 gp120-at felismerõ felszíni eleméhez
Öt poliszulfonált vegyület [Acid Blue 116, Acid Red 115, Direct Yellow 50 (DY50), Direct Red 79 (DR79) és Suramin; lásd Fig. 1. az angol nyelvû szövegben] hatását vizsgáltuk meg a CD4 és az aLeu3a monoklonális antitest közti kölcsönhatásra. Áramlási citometriával vizsgáltuk, hogy a vegyületek mennyiben képesek gátolni a CD4-aLeu3a kötõdést, amely jó modellje a CD4-gp120 felismerési folyamatnak, de technikailag könnyebben kivitelezhetõ. Két, hasonló szerkezeti elemeket tartalmazó (mindkét molekula diszulfonált naftalin gyûrûket tartalmaz), de nagyon különbözõ hatású molekulát, a DR79-et, illetve a DY50-et választottuk ki részletes szerkezeti elemzésre. Lényeges különbség csak a szulfonsav csopotok elhelyezkedésében van, míg a két anionos csoport transz helyzetben van a DY50-ben, cisz- jellegû szubsztitúció található a DR79 esetében. A cisz elrendezõdésnél rövidebb távolságot mértünk, így ezt a geometriai értéket tekintettük a szerkezethatás vizsgálatunk legfontosabb paraméterének. Míg a DR79 (cisz) hatékonyan gátolta a CD4-aLeu3a kötõdést (IC50 = 20 mg/ml) a DY50 (transz) nem mutatott gátló hatást.
Összehasonlítva a DS....S értékeket, a DR79 sokkal pontosabban tud illeszkedni a CD4 DH....H távolságához mint a DY50. MM számításokból a [CD4....DR79] komplex sztérikus energiája 41.48 kcal/mol-lal alacsonyabbnak adódott a [CD4....DY50] komplexénél. Ez a stabilizációs energiatöbblet az erõsebb elektrosztatikus kölcsönhatásból származik.
Néhány poliszulfonált festék szincicium képzõdést gátló hatása
Az azo-festékek csoportjának egy másik figyelemre méltó hatása a szincicium képzõdés gátlása. A szinciciumok több sejmaggal és összeolvadó membrán szerkezettel rendelkezõ T-sejt konglomerátumok, melyek a fertõzött sejtek felszínén expresszált gp120/gp41 komplexek, valamint nem fertõzött CD4+ sejtek találkozásakor jönnek létre. Ez a közvetlen sejt ® sejt vírus transzport a fertõzött sejtek számának ugrásszerû emelkedéséhez vezet.
Az azo-festékek nem csak a CD4 molekulának az aLeu3a monoklonális antitestet kötõ helyén képes gátolni a CD4-gp120 kölcsönhatást. A poliszulfonált molekulák képesek a gp120 V3 régiójához is specifikusan kötõdni. Ez a kettõs hatásmechanizmus magyarázhatja a vizsgált molekulák jelentõs szincicium gátló sajátságát. A DR79 különösen kiemelkedõ inhibíciós hatását azonban csak egy új szerkezeti modell bevezetésével értelmezhettük. Ez a jelenség a mérésekkel illetve számításokkal összhangban CD4-DR79-CD4 komplexek kialakulásával magyarázható.
Peptid inhibítorok szintézise és tervezése
A CD4 biológiai hatását mimikáló ciklopeptidekhez két lizin, egy arginin és egy fenilalanin elengedhetetlenül szükséges. A gp120 negatív karakterû kötõhelyéhez történõ illeszkedésben a ciklopeptidek gyûrûmérete és flexibilitása döntõ fontosságú. A CD4 szerkezetével kapcsolatos illetve ciklopeptideken végzett számítások alapján több peptid szekvencia tûnt szintézisre érdemesnek. Több szintetikus utat összehasonlítva, hét ciklizált illetve galaktozilezett peptidet szintetizáltunk további biológiai vizsgálatok céljára.
On the structural biochemistry of the HIV-host cell interactions Molecular modelling, synthesis and biological investigations of binding-inhibitor molecules
Ph. D. thesis, Albert Szent-Györgyi Medical University
Szeged 1996
The main aim of the present work is to study the structural biological aspects of covering the section of the CD4 receptor surface which serves as the HIV-1 envelope glycoprotein binding site as well as the complementary surface region of the gp120. In this thesis, two possibilities for blocking the CD4....gp120 complex formation were studied:


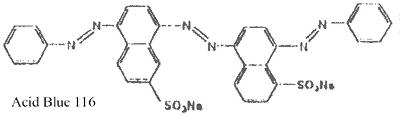


Fig. 1. The structure of polisulfonated dyes and of Suramin
(i) first, the ability of negatively charged molecules to cover the positively charged gp120 binding site on the CD4 was studied. In order to explain of the structure-activity relationships of dyes, the up-to-date molecular modelling tools were applied.
(ii) positively charged cyclopeptides were synthesized in order to mimic the positively charged subdomain of the CD4, on which the negatively charged gp120 segments bind. This family of the cyclic peptides could form a complex with the gp120 by inactivating its binding capacity. In order to elaborate the synthesis of different cyclic- and galactosylated peptides, several possibilities of synthetic methods were tested.
Covering the gp120 binding site on the CD4 surface by polysulfonated dyes
The binding activities of five samples of primarily investigated polysulfonated dyes (Acid Blue 116, Acid Red 115, Direct Yellow 50, Direct Red 79, and Suramin; c.f. Fig.1.) to the CD4 D1 domain were studied by flow cytomety. The structures of the dyes are shown in Figure 1. Initially, we have selected two compounds for molecular modelling due to their structural similarity and their highly different biological activity. The dyes were Direct Red 79 (DR79) and Direct Yellow 50 (DY50). One of the selected two azo-dyes, the DR79 has shown to bind strongly to the CD4 surface, while the DY50 has shown only a marginal affinity.
Both azo-dyes contain disulfonated naphthalene ring moieties. More detailed examination of the dye structures revealed that the two -SO3- moieties are arranged differently in the two azo-dyes. The two -SO3- groups are in trans arrangement in the biologically non-active DY50, while they are in cis arrangement in the biologically active DR79. Interestingly, a shorter S....S distance was found in DY50 than in DR79. The DH....H values (H-H distances between the Lys46 and Arg59 side chains of the CD4) were computed by MD simulations.
Comparing the DS....S values of the two dyes with DH....H, it was shown that the DS....S of DR79 fitted more accurate to DH....H than the shorter DS....S of DY50. According to the MM computation, the [CD4....DR79] complex was found to be more stable than the [CD4....DY50] by 41.48 kcal/mol. This excess stability originates almost exclusively from the electrostatic contribution as might be expected from the interaction of the negatively charged azo-dyes and the positively charged CD4.
Syncytium formation and its inhibition by selected sulfonated dyes
An additional observed biological feature of the azo-dye group is its inhibition ability against the syncytium formation. The syncytia are multinucleated giant cells, one of the typical cytopathic effects caused by different viruses. Such syncytia are also formed between one of the HIV-infected cells and several uninfected lymphocytes. The main reason for this phenomenon is a relative over expression of gp120/gp41 complex in the host cells. This direct (i.e. without virion budding) cell-to-cell transfer of various viral particles (i.e. viral RNA, RT and integrase) can result in a very efficient spread out of the viral infection.
The polysulfonated-azo dye molecules have more possibility to inhibit the above mechanism than they were able to inhibit the complexation between CD4 and aLeu3a monoclonal antibody. Beside the docking of dyes to the D1 domain of CD4, the alternate way to inhibit the syncytium formation is the binding of the sulfonated azo-dyes to the V3 loop of gp120. The result of such quantitation is expressed as percentage of syncytium formation. The extent of the inhibition, measured as the reduction of syncytium forma-tion. The DR79 had been proven to be the best inhibitor against syncytia formation. To explain its outstanding inhibitor ability, a new model was established. The suggested mechanism at the molecular level is the formation of an CD4-DR79-CD4 trimer structure.
Design and synthesis of peptide analogues as docking inhibitors
It is proposed, that two lysine, one arginine, and one phenylalanine residues are essential requirements in a cyclopeptide for mimicking the biological activity of the CD4. The ring size of the cyclopeptide is crucial so that it may fit into the negatively charged cavity of the gp120. The location of these four amino acids in the cyclopeptide is also crucial because it should mimic the geometrical arrangements of these four amino acid side chains in the CD4 molecule. Several cyclic and galactosylated peptide derivatives were synthesized for further biological investigations.
Publications
1. Zoltán Székely, András Perczel, Botond Penke and József Molnár: A new method for the interpretation of dynamics trajectories in the conformational analysis of HIV receptor mutants, Journal of Molecular Structure (Theochem), 286 (1992) 165-182
2. Zoltán Székely, András Perczel, Botond Penke, József Molnár and Adorján Aszalós: Molecular dynamic simulation indicate conformational changes in Asn52 CD4 mutants Journal of Cellular Biochemistry, Suppl. 18/B. (1994) P125.
3. Zoltán Székely: A new approach for an HIV docking-inhibitor drug designed on the basis of the dual recognition/binding hypothesis between the CD4 receptor and the envelope glycoprotein of the HIV Journal of Molecular Structure (Theochem), 334 (1995) 93-100
4. Zoltán Székely, Zoltán Kónya, Attila Becskei, William P.D. Goldring, András Perczel, Botond Penke, József Molnár, Adorján Aszalós and Imre G. Csizmadia: Suggested binding mechanism of the HIV-gp120 to its CD4 receptor Journal of Molecular Structure (Theochem), 367 (1996) 159-186
5. Zoltán Székely, László Torday, Christopher J. Michejda and Adorján Aszalós: Binding between the CD4 receptor and polysulfonated azo-dyes. An exploratory theoretical study on action-mechanism Journal of Molecular Structure (Theochem), (accepted)
| Vissza a tartalomjegyzékhez Back to Contents |
http://www.kfki.hu/chemonet/ http://www.ch.bme.hu/chemonet/ |